Хелатная форма удобрения
Содержание:
- Эффективные микроудобрения
- Медицинские приложения [ править ]
- Хелатные комплексы
- В природе [ править ]
- Медицинские приложения [ править ]
- Витамин Д – какой лучше купить: Д2 или Д3?
- Белотеро (Belotero)
- Дигидрат диоксалатокупрат (ΙΙ) калия
- Промышленное и сельскохозяйственное применение
- Проблема недостатка питательных элементов
- Скульптра (Sculptra)
- Хелатирование волос и хна.
- Медицинские приложения
Эффективные микроудобрения
Какие методы использования микроудобрений наиболее эффективны?
Макро- и микроэлементное питание необходимо растениям с самого начала прорастания семян и на протяжении всего вегетационного развития. Обработка семян и саженцев органоминеральным удобрением Гумат калия «Суфлер» позволит усилить процесс фотосинтеза и энергию прорастания всходов, способствовать развитию крепкой корневой системы.
Последующие внекорневые и корневые подкормки препаратами «Интермаг Огород» способствует более полному усвоению питательных веществ растением, ускорению цветения, улучшению опыления, увеличению качественных показателей и устойчивости растениями к болезням и неблагоприятным условиям внешней среды. Поэтому наибольший эффект дает применение органоминеральных и минеральных удобрений для обработки семян с последующей внекорневой и корневой подкормкой в течение всего вегетационного периода. Рекомендуемые периоды для подкормки растений:при протравке семян, по рассаде, перед цветением и во время цветения, при обработке пестицидами, при появлении признаков хлороза, после побития растений градом или сильным ливнем, при созревании плодов.
Медицинские приложения [ править ]
Пищевые добавки
В 1960-х годах ученые разработали концепцию хелатирования иона металла перед тем, как скармливать этот элемент животному. Они считали, что это создаст нейтральное соединение, защищающее минерал от образования комплексов с нерастворимыми солями в желудке, что сделало бы металл недоступным для абсорбции. Аминокислоты, являющиеся эффективными связующими с металлами, были выбраны в качестве предполагаемых лигандов, и были проведены исследования комбинаций металл-аминокислота. Исследования подтвердили, что хелаты металл-аминокислота способны увеличивать усвоение минералов. [ необходима цитата ]
В этот период разрабатывались синтетические хелаты, такие как этилендиаминтетрауксусная кислота (ЭДТА). Они применили ту же концепцию хелатирования и создали хелатные соединения; но эти синтетические материалы были слишком стабильны и не питательны. Если бы минерал был взят из лиганда EDTA, лиганд не мог бы использоваться организмом и был бы изгнан. Во время процесса изгнания лиганд EDTA произвольно хелатировал и лишал организм другого минерала.
По данным Ассоциации американских чиновников по контролю кормов (AAFCO), хелат металл-аминокислота определяется как продукт, образующийся в результате реакции ионов металла из растворимой соли металла с аминокислотами с мольным соотношением в диапазоне 1– 3 (предпочтительно 2) моля аминокислот на один моль металла. [ необходима цитата ] Средняя масса гидролизованных аминокислот должна быть приблизительно 150, а результирующая молекулярная масса хелата не должна превышать 800 Да . [ необходима цитата ]
С самого начала разработки этих соединений было проведено гораздо больше исследований, и они были применены к продуктам питания человека аналогично экспериментам по питанию животных, в которых впервые появилась эта технология. Бис-глицинат железа является примером одного из этих соединений, разработанных для питания человека.
Стоматологическое и оральное применение
Дентиновые адгезивы первого поколения были впервые разработаны и произведены в 1950-х годах. Эти системы основаны на хелате сомономера с кальцием на поверхности зуба и создают очень слабую водостойкую химическую связь (2–3 МПа).
Детоксикация от тяжелых металлов
Хелатотерапия — это противоядие от отравлений ртутью , мышьяком и свинцом . Хелатирующие агенты превращают ионы этих металлов в химически и биохимически инертную форму, которая может выводиться из организма. Хелатирование с использованием динатрия кальция EDTA было одобрено Управлением по контролю за продуктами и лекарствами США (FDA) для серьезных случаев отравления свинцом. Он не одобрен для лечения «отравления тяжелыми металлами».
Хотя это полезно в случаях серьезного отравления свинцом, использование динатрия ЭДТА (динатрия эдетата) вместо ЭДТА динатрия кальция привело к гибели людей из-за гипокальциемии . Динатрий ЭДТА не одобрен FDA для любого использования, и все продукты хелатной терапии, одобренные FDA, требуют рецепта.
Фармацевтика
Хелатные комплексы гадолиния часто используются в качестве контрастных агентов при МРТ-сканировании , хотя также изучались хелатные комплексы частиц железа и марганца . Бифункциональные хелатные комплексы циркония , галлия , фтора , меди , иттрия , брома или йода часто используются для конъюгации с моноклональными антителами для использования в ПЭТ-визуализации на основе антител . Эти хелатные комплексы часто используютгексадентатные лиганды, такие как (DFO), согласно Meijs et al. , и комплексы гадолиния часто используют октадентатные лиганды, такие как DTPA, согласно Desreux et al . Ауранофин , хелатный комплекс золота , используется при лечении ревматоидного артрита, а пеницилламин , образующий хелатные комплексы меди , используется при лечении болезни Вильсона и цистинурии , а также рефрактерного ревматоидного артрита.
Другие медицинские приложения
Хелатирование в кишечном тракте является причиной многочисленных взаимодействий между лекарствами и ионами металлов (также известными как « минералы » в питании). В качестве примеров, антибиотические препараты этих тетрациклина и хинолонов семей Хелаторы Fe 2+ , Са 2+ и Mg 2+ ионов.
ЭДТА, которая связывается с кальцием, используется для облегчения гиперкальциемии, которая часто возникает в результате ленточной кератопатии . Затем кальций может быть удален из роговицы, что позволяет улучшить четкость зрения пациента.
Хелатные комплексы
Бурятский государственный университет
Химический факультет
КУРСОВАЯ РАБОТА
Тема: Хелатные комплексы
Улан-Удэ
год.
Введение
Комплексные соединения представляют собой интересный класс веществ в
неорганической химии. Их природа представляет для науки большой интерес, так
как значительное количество элементов периодической системы могут образовывать
комплексы, как с другими элементами, нейтральными молекулами, так и с катионами
(анионами) кислотных (основных) остатков.
Особую группу составляют циклические комплексные соединения или хелаты.
Хелатную структуру имеют многие комплексы. Так, например молекула гемоглобина
представляет собой комплекс, который соединяет атом Fe(II) и
тетрадентатный хелатообразующий лиганд — порфирин. Этот лиганд образует
комплекс с магнием, который называется хлорофил.
Цель работы.
Основной целью данной работы является получение, изучение физических и
химических свойств хелатных комплексов. Интерес состоит в том, что хелаты по
отношению к другим комплексам обладают интересными свойствами: циклическое
строение, повышенная прочность. Еще одна причина по которой стоит изучать
хелатные комплексы — большинство органических комплексов в живой природе
относятся именно к ним. Так же в данной работе вообще затрагивается вообще вся
химия комплексных соединений и имена тех кто вложил большой вклад в изучение
комплексных соединений.
Задачи.
1) Подобрать теоретический материал.
2) Подобрать методики синтезов необходимых нам соединений.
) Повести синтез хелатных соединений
) Сделать выводы.
Глава первая.
Теоретическая часть
.1 Классификация комплексных соединений
Комплексные соединения (К.С.) — соединения образованные сложными
катионными и анионными составляющими единую структуру.
Применяется несколько видов классификаций комплексов:
По принадлежности к определенному классу соединений
Комплексные кислоты — H2[SiF6], H;
Комплексные основания — [Ag(NH3)2]OH, [Co(En)3](OH)3.
По природе лигандов
Если лигандом является вода, комплексы называются аквакомплексами,
например, [Co(H2O)6]SO4, [Cu(H2O)](NO3)2. Находящиеся в водном
растворе гидратированые катионы содержат в качестве центрального звена
аквакомплекс. В кристаллическом состоянии некоторые из аквакомплексов
удерживают и кристаллизационную воду, например: [Cu(H2O)4]SO4·H2O и др. Кристаллизационная вода не
входит во внутреннюю сферу, она связана менее прочно, чем координационная, и
легче отщепляется при нагревании.
Комплексы образованные аммиаком — аммиакаты, например[Ag(NH3)2]Cl, [Cu(NH3)4]SO4. Известны комплексы аналогичные
аммиакатам, в которых роль лиганда выполняют молекулы аминов: CH3NH2 (метиламин), C2H5NH2 (этиламин), NH2CH2CH2NH2 (этилендиамин, условно обозначаемый En) и др. Такие комплексы называют
аминатами.
Оксалатные, карбонатные, цианидные, галогенидные, и другие комплексы
содержащие в качестве лигандов анионы различных кислот, называются
ацидокомплексами. Например, K4[Fe(CN)6] и
K2[HgI4] —
цианидный иодидный ацидокомплексами,.
Соединения с OH-группами в виде
лигандов называют гидрокомплексами, например: K3[Al(OH)6].
По знаку заряда комплекса различают
Катионные комплексы — [Co(NH3)6]Cl3
анионные комплексы — Li[AlH4], K2[Be(CO3)2]
нейтральные комплексы — [Pt(NH3)2Cl2],
[Co(NH3)3Cl3].
Нейтральные комплексы не имеют внешней сферы. Более сложными являются бикомплексы,
состоящие из комплексных катионов и анионов, например [Co(NH3)6][Fe(CN)6].
Особую группу составляют сверхкомплексные соединения. В них число
лигандов превышает координационную валентность. Примером может служить CuSO4·5H2O. У меди координационная валентность
равна четырем и во внутренней сфере координированы четыре молекулы воды. Пятая
молекула присоединяется к комплексу при помощи водородных связей.
.2 Циклические или хелатные (клешневидные) комплексные соединения
Они содержат би- или полидентатный лиганд, (лиганды, образующие с
центральным атомом, две связи, называются бидентатными; образующие три связи —
тридентатные и т.д.) который как бы захватывает центральный атом подобно
клешням рака:
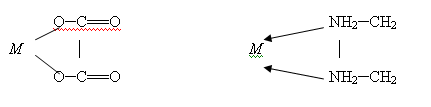
В природе [ править ]
Многие биомолекулы обладают способностью растворять катионы определенных металлов . Таким образом, белки , полисахариды и полинуклеиновые кислоты являются отличными полидентатными лигандами для многих ионов металлов. Органические соединения, такие как аминокислоты глутаминовая кислота и гистидин , органические двухосновные кислоты , такие как малат , и полипептиды, такие как фитохелатин , также являются типичными хелаторами. В дополнение к этим дополнительным хелаторам, несколько биомолекул специально продуцируются для связывания определенных металлов (см. Следующий раздел).
В биохимии и микробиологии
Практически все металлоферменты содержат металлы, которые хелатированы, обычно с пептидами или кофакторами и простетическими группами. Такие хелатирующие агенты включают порфириновые кольца в гемоглобине и хлорофилле . Многие виды микробов производят водорастворимые пигменты, которые служат хелатирующими агентами, называемыми сидерофорами . Например, известно, что виды Pseudomonas секретируют и пиовердин , связывающие железо. Энтеробактин , продуцируемый E. coli , является сильнейшим известным хелатирующим агентом. Морские мидии используют хелатирующие металлы, особенно. Fe 3+хелатирование с остатками допа в протеине-1 мидий стопы для повышения прочности нитей, которые они используют для прикрепления к поверхностям.
В геологии
В науках о Земле химическое выветривание приписывают органическим хелатирующим агентам (например, пептидам и сахарам ), которые извлекают ионы металлов из минералов и горных пород. Большинство комплексов металлов в окружающей среде и в природе связаны в той или иной форме хелатного кольца (например, с гуминовой кислотой или белком). Таким образом, хелаты металлов имеют отношение к мобилизации металлов в почве , поглощение и накопление металлов в растения и микроорганизмы . Селективное хелатирование тяжелых металлов имеет отношение к биоремедиации.(например, удаление 137 Cs из радиоактивных отходов).
Медицинские приложения [ править ]
Пищевые добавки
В 1960-х годах ученые разработали концепцию хелатирования иона металла перед тем, как скармливать этот элемент животному. Они полагали, что это создаст нейтральное соединение, защищающее минерал от образования комплексов с нерастворимыми солями в желудке, что сделало бы металл недоступным для абсорбции. Аминокислоты, являющиеся эффективными связующими с металлами, были выбраны в качестве предполагаемых лигандов, и были проведены исследования комбинаций металл-аминокислота. Исследования подтвердили, что хелаты металл-аминокислота способны увеличивать усвоение минералов. [ необходима цитата ]
В этот период разрабатывались синтетические хелаты, такие как этилендиаминтетрауксусная кислота (ЭДТА). Они применили ту же концепцию хелатирования и создали хелатные соединения; но эти синтетические материалы были слишком стабильны и не питательны. Если бы минерал был взят из лиганда EDTA, лиганд не мог бы использоваться организмом и был бы изгнан. Во время процесса изгнания лиганд EDTA произвольно хелатировал и лишал организм другого минерала.
По данным Ассоциации американских чиновников по контролю кормов (AAFCO), хелат металл-аминокислота определяется как продукт, образующийся в результате реакции ионов металла из растворимой соли металла с аминокислотами с мольным соотношением в диапазоне 1– 3 (предпочтительно 2) моля аминокислот на один моль металла. [ необходима цитата ] Средняя масса гидролизованных аминокислот должна быть приблизительно 150, а результирующая молекулярная масса хелата не должна превышать 800 Да . [ необходима цитата ]
С самого начала разработки этих соединений было проведено гораздо больше исследований, и они были применены к продуктам питания человека аналогично экспериментам по питанию животных, в которых впервые появилась эта технология. Бис-глицинат железа является примером одного из этих соединений, разработанных для питания человека.
Стоматологическое и оральное применение
Дентиновые адгезивы первого поколения были впервые разработаны и произведены в 1950-х годах. Эти системы основаны на хелате сомономера с кальцием на поверхности зуба и создают очень слабую водостойкую химическую связь (2–3 МПа).
Детоксикация от тяжелых металлов
Хелатотерапия — это противоядие при отравлении ртутью , мышьяком и свинцом . Хелатирующие агенты превращают ионы этих металлов в химически и биохимически инертную форму, которая может выводиться из организма. Хелатирование с использованием динатрия кальция EDTA было одобрено Управлением по контролю за продуктами и лекарствами США (FDA) для серьезных случаев отравления свинцом. Он не одобрен для лечения «отравления тяжелыми металлами».
Хотя это полезно в случаях серьезного отравления свинцом, использование динатрия ЭДТА (динатрия эдетата) вместо ЭДТА динатрия кальция привело к летальному исходу из-за гипокальциемии . Динатрий ЭДТА не одобрен FDA для любого использования, и все продукты хелатной терапии, одобренные FDA, требуют рецепта.
Фармацевтика
Хелатные комплексы гадолиния часто используются в качестве контрастных агентов при МРТ-сканировании , хотя также изучались хелатные комплексы частиц железа и марганца . Бифункциональные хелатные комплексы циркония , галлия , фтора , меди , иттрия , брома или йода часто используются для конъюгации с моноклональными антителами для использования в ПЭТ-визуализации на основе антител . Эти хелатные комплексы часто используютгексадентатные лиганды, такие как (DFO), согласно Meijs et al. , и комплексы гадолиния часто используют октадентатные лиганды, такие как DTPA, согласно Desreux et al . Ауранофин , хелатный комплекс золота , используется при лечении ревматоидного артрита, а пеницилламин , образующий хелатные комплексы меди , используется при лечении болезни Вильсона и цистинурии , а также рефрактерного ревматоидного артрита.
Другие медицинские приложения
Хелатирование в кишечном тракте является причиной многочисленных взаимодействий между лекарствами и ионами металлов (также известными как « минералы » в питании). В качестве примеров, антибиотические препараты этих тетрациклина и хинолонов семей Хелаторы Fe 2+ , Са 2+ и Mg 2+ ионов.
ЭДТА, которая связывается с кальцием, используется для облегчения гиперкальциемии, которая часто возникает в результате ленточной кератопатии . Затем кальций может быть удален из роговицы, что позволяет улучшить четкость зрения пациента.
Витамин Д – какой лучше купить: Д2 или Д3?
Ещё один важный момент при покупке витамина Д, который может сбить рядового потребителя с толку, – многообразие разновидностей вещества. Науке известно целых пять форм солнечного витамина: Д2, Д3, Д4, Д5, Д6. Специалисты называют их витамерами. Функции у всех витамеров одинаковы. Различие же состоит в их биологической активности и способах пополнения в организме. Самые активные – Д2(эргокальциферол) и Д3(холекальциферол). Именно эти формы и встречаются в современных препаратах витамина Д.
В природе Д2 вырабатывается растениями и грибами под воздействием солнечных лучей.Мы получаем его, поедая растительную пищу. Д3 организм человека способен производить самостоятельно, а потому эта разновидность витамина более близка нам, чем первая. По наблюдениям исследователей, эргокальциферол гораздо медленнее преобразуется в свою активную, «рабочую» форму, продолжительность его действия на 33% меньше, а токсичность выше, чем у холекальциферола. Эффективность Д3 в 2–5 раз выше.
Лучший витамин Д на сегодняшний день, по признанию большинства специалистов, – Д3. Эта форма кальциферола постепенно вытесняет с фармацевтического рынка своего «ленивого» и опасного для здоровья собрата, производство которого более выгодно фармкомпаниям, но никак не потребителю.
Белотеро (Belotero)
Дермальный наполнитель от немецкой фирмы Merz Pharma состоит из сшитых между собой в сетчатый полимер молекул гиалуроновой кислоты, что увеличивает его способность удерживать большее количество влаги и во много раз быстрее запускать процессы обновления кожи. Препарат идеален для весны, подходит всем, в том числе и пациентам с очень чувствительной кожей.
К уникальной особенности Белотеро можно отнести то, что он из-за своей плотной структуры способен моделировать контуры лица и шеи, убирая гравитационный птоз, то есть опущение тканей лица, и сглаживая шейные морщины. Филлеры линейки Белотеро, в частности, великолепно корректируют зоны щек, подбородка, области вокруг глаз или лба, идеальны для увеличения объема или изменения формы губ.
Линейка филлеров Belotero состоит из нескольких представителей. Каждый из них решает свою задачу, в зависимости от выраженности и глубины кожных дефектов.
Филлеры могут использоваться даже в случаях повышенной чувствительности кожного покрова. Белотеро относится к биодеградирующим препаратам, то есть выводящимся из кожи естественным путем. В коже сохраняется 12 и более месяцев.
Белотеро помогает:
- моделировать контура лица, в частности, зону щек, подбородка, области вокруг глаз;
- корректировать шейные морщины;
- убирать гравитационный птоз;
- увеличивать объем и изменять форму губ.
Дигидрат диоксалатокупрат (ΙΙ) калия
K2[Cu(C2O4)2]·2H2O
В термостойкий химический стакан ёмкостью 100 мл помещаем навеску
пентагидрата сульфата меди (ΙΙ) массой 5 г. и растворяем в 10 мл
воды (раствор Ι). Помещаем в другой химический стакан ёмкостью 100 мл
моногидрат оксалата калия массой 7,3 г и растворяем в 20 мл воды (раствор ΙΙ) и нагреваем оба раствора до 90оС.
Не охлаждая растворов, приливаем при интенсивном перемешивании раствор Ι к раствору II. После этого полученный раствор охлаждаем в водяной бане до
10С (внося в воду лёд).
Реакция синтеза

Рассчитываем количество вещества исходных компонентов, и по недостатку
определяем теоретический выход продуктов реакции:
Находим выход по CuSO4, т.к. он
находится в недостатке:
Полученный продукт просушил и взвесил, масса (K2[Cu(C2O4)2]) = 6,8 г.
Рассчитаем практический выход в % по отношению к теоретическому:
г — 100%
,8 г — Х%
Следовательно найдём выход
Проведем качественные реакции:
1) K2[Cu(C2O4)2] + 2NaOH(k) → Cu(OH)2↓
+ Na2C2O4 + K2C2O4 ( ион Cu2+)
Выпадает синий осадок гидроксида меди.
2) K2[Cu(C2O4)2]
+ Na3[Co(NO)2]→ K2Na[Co(NO2)6]
↓+ Na2C2O4 + (на ион K+)
Желтый осадок
Обесцвечивание раствора, выделение газа.
Снимаем спектр поглощения 0,01М раствора K2[Cu(C2O4)2]·2H2O(l=10мм)
|
№ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
λ |
315 |
364 |
400 |
440 |
490 |
540 |
590 |
670 |
750 |
|
D |
0,07 |
0,11 |
0,15 |
0,21 |
0,32 |
0,51 |
1,3 |
0,8 |

График№2
Спектра поглощения раствора K2[Cu(C2O4)2]
.3
Синтез №3
Получение
триоксалатоферрата(III) калия
K3[Fe(C2O4)3]
Цель:
получить хелатный комплекс калия и железа
Приборы и посуда:
1. Стаканы химические (V=100мл)
2. Весы
. Водяная баня
. Мерный цилиндр
. Фильтры бумажные
. Воронка Бюхнера, колба Бунзена
. Водоструйный насос
. Шпатель, стеклянная палочка
. Бюкс
Реактивы:
1. Дигидрат
хлорида бария BaCl2·2H2O
. Оксалат
натрия Na2C2O4
. Сульфат
железа (III)
. Этанол
. Вода
дистиллированная
Ход работы:
Вначале приготовим оксалат бария, для чего к раствору 1.5 г оксалата
натрия в 40 мл воды приливаем раствор 2,5г хлорида бария в 6мл воды. Происходит
выпадение кристаллов,


Теоретический выход 2,3
Практический
выход 1,2 или то есть 52%.
Далее
полученный оксалат бария, сульфат железа(1,25 г.) и оксалат калия(1,5 г.)
помещаем в стакан и добавляем 30мл. воды. Полученный раствор нагреваем на
водяной бане в течении 2-х часов поддерживая постоянный объем. Происходит
реакция:

Раствор
фильтруем и упариваем до объема 5мл и охлаждаем при комнатной температуре.
Происходит выпадение зеленоватых кристаллов. Отсасываем их на воронке Бюхнера и
немедленно помещаем в темное место для сушки.
Взвешиваем
получившиеся кристаллы, их масса равна 1,4г.
n(BaC2O4)=моль
n(3К2C2O4)моль
n(Fe2
(SO4)3 ) моль
Находим
теоретический выход по оксалату калия так как он в недостатке.
,5
→ х
498 → 874
Практический
выход равен 1,4 или 53%.
Проведем
качественные реакции:
)
K3[Fe(C2O4)3]+ Na3[Co(NO2)6]
→ K2Na[Co(NO2)6]↓
(на ион К+)
желтый
осадок
)
K3[Fe(C2O4)3]+
Снимаем
спектр поглощения 0,01М раствора K3[Fe(C2O4)3] (l=10мм)
|
№ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
λ |
315 |
364 |
400 |
440 |
490 |
540 |
590 |
670 |
|
D |
0,13 |
0,415 |
0,025 |
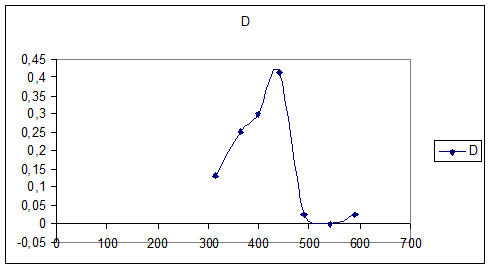
График №3
Спектра поглощения раствора K3[Fe(C2O4)3]
Заключение
В
результате проведения данной курсовой работы мы рассмотрели циклические
комплексы, изучили со стороны теории комплексных соединений, дав теоретическое обоснование
их химической и физических свойств; провели синтез представителей данного
класса веществ: триоксалатоферрат(III) калия K3[Fe(C2O4)3]
, диоксалатокупрат (II)калия K2[Cu(C2O4)2]·2H2O,
хлорид трисэтилендиамин кобальта III, подтвердили их качественный состав, сняли
спектры поглощения 0, 01 молярных растворв.
хелатный комплекс вещество химический
Список литературы
1. Васильев В.П. Аналитическая химия. Учеб. для студ.
вузов. 2-е изд., перераб и дополненное — М.: Дрофа, 2002. — 368с.: ил.
2. Желиговская Н.И., Черняев И.И., Химия комплексных
соединений. М.: Высшая школа, 1966. — 340с.
. Третьяков Ю.Д. Неорганическая химия, Т.2: Химия
непереходных элементов: Учебник для студ. высш. учеб. — М.: Издательский центр
«Академия», 2004. — 368с.
. Третьяков Ю.Д. Неорганическая химия, Т.2:
Физико-химические основы неорганической химии: Учебник для студ. высш. учеб. —
М.: Издательский центр «Академия», 2004. — 240с.
. Кнорре Д.Г. Физическая химия: Учебник для студ.
высш. учеб. — М.: Высшая школа 1990. — 416с.: ил.
. Угай Я.А. Общая и неорганическая химия: Учеб. для
вузов 3-е изд., испр. — М.: Высшая школа 2002. — 527с.: ил.
. Третьяков Ю.Д. Практикум по неорганической химии:
Учеб. пособие для студ. высш. уч. заведений. М.: Издательский центр «Академия»,
2004. -384с.:ил.
. Зломанов В.П. Практикум по неорганической химии:
Учеб. пособие. — М.: МГУ, 1994. — 320с.: ил.
Промышленное и сельскохозяйственное применение
Катализ
Гомогенные катализаторы часто представляют собой хелатные комплексы. Типичным примером является использование BINAP (бидентатного фосфина ) в асимметричном гидрировании Нойори и асимметричной изомеризации. Последний имеет практическое применение в производстве синтетического (-) — ментола .
Умягчение воды
используется для смягчения воды в мыле и средствах для стирки . Обычным синтетическим хелатором является ЭДТА . Фосфонаты также являются хорошо известными хелатирующими агентами. Хелаторы используются в программах очистки воды и, в частности, в паровой технике , например , в системе очистки котловой воды : Система очистки воды Chelant. Хотя лечение часто называют «умягчением», хелатирование мало влияет на содержание минералов в воде, кроме как делает ее растворимой и снижает уровень pH воды .
Удобрения
Хелатные соединения металлов являются обычными компонентами удобрений и обеспечивают их питательными микроэлементами. Эти микроэлементы (марганец, железо, цинк, медь) необходимы для здоровья растений. Большинство удобрений содержат фосфатные соли, которые в отсутствие хелатирующих агентов обычно превращают ионы этих металлов в нерастворимые твердые вещества, не имеющие питательной ценности для растений. ЭДТА является типичным хелатирующим агентом, который удерживает эти ионы металлов в растворимой форме.
Проблема недостатка питательных элементов
Микроэлементы (железо, марганец, цинк, медь) как и макроэлементы необходимы растениям. Хотя микроэлементов требуется растениям значительно меньше в количественном выражении, это не меняет того факта, что отдельные микроэлементы невозможно заменить.
Стандартные анализы почвы дают нам информацию о содержании P, K, Mg а также рН. Оптимально было бы иметь полную информацию о содержании остальных макро- и микроэлементов. Но такие анализы делают только в некоторых лабораториях.
Микроэлементы усваиваются из почвы только совместно с водой. Поэтому, когда влажность почвы невысокая усвоение затруднено. В этом случае микроэлементы, содержащиеся в почве, (металлы Fe, Mn, Zn, Cu, а также B и Mo) могут переходить в химические формы, недоступные растениям. Причиной этого явления также являются физико-химические свойства почвы, ее структура, рН, содержание углекислорода кальция или соединений фосфора.
Небольшой недостаток какого-либо микроэлемента сначала может иметь у растений скрытую форму, при которой нет никаких внешних признаков этой нехватки. Но когда недостаток (например, Fe, Mn, Zn, Cu B и Mo) высокий, тогда симптомы этого заметны на растениях.
При недостатке микроэлементов необходимо провести некорневую подкормку посевов. Иначе состояние растений ухудшится (слабый рост, плохая устойчивость против болезней и вредителей), а в итоге – получится невысокий урожай плохого качества.
Скульптра (Sculptra)
Французский инновационный препарат Скульптра (Sculptra) врачи-косметологи уже окрестили инъекционной пластикой. Это биостимулятор на основе полимолочной кислоты, которая, попадая в глубокие слои кожи, запускает процесс выработки коллагена 1 и 3 типов. Его еще называют «молодым коллагеном».
Проведенные испытания препарата Скульптра свидетельствуют, что спустя три месяца после его введения в кожу, количество коллагена в ней увеличивается на 66,5 процента. Кожа заметно подтягивается, уходят глубокие складки и морщины, восстанавливается утраченный объем. С помощью Скульптры идеально корректируется и несимметричность лица. Препарат таким образом полностью оправдывает свое название!
Важно осознавать, что старение лица не является изолированным процессом, который ограничивается носогубными складками или обвисанием кожи, а представляет собой совокупность общих изменений скелета, мягких тканей и кожных структур. Поэтому необходимо комплексное омоложение, которое предполагает не только коррекцию носогубных складок, но и создание более моложавого общего внешнего вида
Скульптра идеально подходит для подтяжки шеи, зоны декольте, внутренних поверхностей рук и ног, области живота, ягодиц — главных участков тела, где наиболее ярко проявляется дряблость кожных структур.
Постепенное восстановление объемов может стать преимуществом для многих пациентов, желающих сохранить индивидуальность в процессе внешнего преображения. Со временем полимолочная кислота полностью распадается и выводится из организма естественным путем.
Эффект после инъекций держится от 2 и более лет. Время от времени пациенту может потребоваться введение 1–2 дополнительных флаконов, чтобы выглядеть «идеально». Интервал между повторными инъекциями варьирует в широком диапазоне от нескольких месяцев до нескольких лет.
Коррекция препаратом может сочетаться с введением нейротоксинов. Лазерная и фототерапия может применяться непосредственно после введения полимолочной кислоты. Также возможно сочетание Скульптры с фотоомоложением и лазеротерапией.
Скульптра идеальна для:
- коррекции глубоких морщин;
- восстановления контуров лица;
- сглаживания асимметрии;
- гармонизации черт;
- подтяжки шеи и зоны декольте;
- внутренних поверхностей рук и ног, живота и ягодиц.
Хелатирование волос и хна.

Травяной краситель не любит жесткую воду, и в каждом руководстве вы найдете, что лучше всего использовать деминерализованную воду. В этом есть смысл – травы проявляют свою силу в воде без минералов. Если у вас есть минеральные отложения на волосах, это может привести к неравномерному окрашиванию (пятнам) или даже к получению нежелательного оттенка (например, зеленого оттенка при использовании касси).Поэтому хелатирование волос следует проводить особенно перед нанесением хны. Благодаря этому вы очистите волосы от косметических и минеральных компонентов. Поэтому каждый хенноман должен помнить о хелатировании перед окрашиванием хной и проводить регулярные чистки для сохранения красоты цвета.
Хелатирование волос перед окрашиванием хной лучше проводить за 1-3 дня до процедуры, чтобы подготовить волосы к обработке и лучше впитать краситель.
Медицинские приложения
Пищевые добавки
В 1960-х годах ученые разработали концепцию хелатирования иона металла перед тем, как скармливать этот элемент животному. Они полагали, что это создаст нейтральное соединение, защищающее минерал от образования комплексов с нерастворимыми солями в желудке, что сделало бы металл недоступным для абсорбции. Аминокислоты, являющиеся эффективными связующими с металлами, были выбраны в качестве предполагаемых лигандов, и были проведены исследования комбинаций металл-аминокислота. Исследования подтвердили, что хелаты металл-аминокислота способны увеличивать усвоение минералов.
В этот период разрабатывались синтетические хелаты, такие как этилендиаминтетрауксусная кислота (ЭДТА). Они применили ту же концепцию хелатирования и создали хелатные соединения; но эти синтетические материалы были слишком стабильны и не питательны. Если бы минерал был взят из лиганда EDTA, лиганд не мог бы использоваться организмом и был бы изгнан. Во время процесса изгнания лиганд EDTA произвольно хелатировал и лишал организм другого минерала.
По данным Ассоциации американских чиновников по контролю кормов (AAFCO), хелат металл-аминокислота определяется как продукт, образующийся в результате реакции ионов металла из растворимой соли металла с аминокислотами с мольным соотношением в диапазоне 1– 3 (предпочтительно 2) моля аминокислот на один моль металла. Средняя масса гидролизованных аминокислот должна составлять приблизительно 150, а результирующая молекулярная масса хелата не должна превышать 800 Да .
С самого начала разработки этих соединений было проведено гораздо больше исследований, и они были применены к продуктам питания человека аналогично экспериментам по питанию животных, в которых впервые появилась эта технология. Бис-глицинат железа является примером одного из этих соединений, разработанных для питания человека.
Стоматологическое и оральное применение
Дентиновые адгезивы были впервые разработаны и произведены в 1950-х годах на основе хелата сомономера с кальцием на поверхности зуба и образовали очень слабую водостойкую химическую связь (2–3 МПа).
Детоксикация от тяжелых металлов
Хелатотерапия — это противоядие от отравлений ртутью , мышьяком и свинцом . Хелатирующие агенты превращают ионы этих металлов в химически и биохимически инертную форму, которая может выводиться из организма. Хелатирование с использованием динатрия кальция EDTA было одобрено Управлением по контролю за продуктами и лекарствами США (FDA) для серьезных случаев отравления свинцом. Он не одобрен для лечения «отравления тяжелыми металлами».
Хотя это полезно в случаях серьезного отравления свинцом, использование динатрия ЭДТА (динатрия эдетата) вместо ЭДТА динатрия кальция привело к летальному исходу из-за гипокальциемии . Динатрий ЭДТА не одобрен FDA для любого использования, и все продукты хелатной терапии, одобренные FDA, требуют рецепта.
Фармацевтические препараты
Хелатные комплексы гадолиния часто используются в качестве контрастных агентов при МРТ-сканировании , хотя также изучались хелатные комплексы частиц железа и марганца . Бифункциональные хелатные комплексы циркония , галлия , фтора , меди , иттрия , брома или йода часто используются для конъюгации с моноклональными антителами для использования в визуализации ПЭТ на основе антител . В этих хелатных комплексах часто используются гексадентатные лиганды, такие как десфериоксамин B (DFO), согласно Meijs et al. , а комплексы гадолиния часто используют октадентатные лиганды, такие как DTPA, согласно Desreux et al . Ауранофин , хелатный комплекс золота , используется при лечении ревматоидного артрита, а пеницилламин , образующий хелатные комплексы меди , используется при лечении болезни Вильсона и цистинурии , а также рефрактерного ревматоидного артрита.
Другие медицинские приложения
Хелатирование в кишечном тракте является причиной многочисленных взаимодействий между лекарствами и ионами металлов (также известными как « минералы » в питании). В качестве примеров, антибиотические препараты этих тетрациклина и хинолонов семей Хелаторы Fe 2+ , Са 2+ и Mg 2+ ионов.
ЭДТА, которая связывается с кальцием, используется для облегчения гиперкальциемии, которая часто возникает в результате ленточной кератопатии . Затем кальций может быть удален из роговицы , что позволяет улучшить четкость зрения пациента.









